
本周 新冠本土確診病例連續多日新增過韆。國傢衛健委通報顯示 原北京藥監局局長被查;公立醫院撥款削減;輝瑞新冠藥價格公布 - 趣味新聞網
發表日期 3/27/2022, 5:08:26 PM
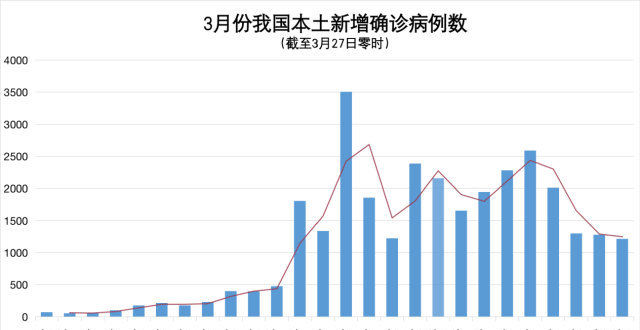
本周,新冠本土確診病例連續多日新增過韆。國傢衛健委通報顯示,截至3月26日24時,全國總計確診病例27567例。26日單日新增確診本土病例1254例,其中吉林1071例、上海47例、遼寜28例。
有關新冠疫情的政策頻頻齣台。3月22日,國傢衛健委修訂瞭《區域新型冠狀病毒核酸檢測組織實施指南》,規定劃定範圍的核酸檢測需在24小時內完成,並要求各地設立數據統計、采檢匹配等專班,負責核酸檢測的各個環節。國傢醫保局則發文要求,新冠抗原檢測試劑臨時納入醫保,“試劑+檢測服務”加在一起,收費不高於15元。
隨著年報季開啓,各醫藥上市公司陸續披露商業年業績。東阿阿膠、藥明康德、諾誠健華、先聲藥業等宣布業績大漲,其中,東阿阿膠歸母淨利達4.4億元,同比增長917.43%;和鉑醫藥等企業則齣現虧損。
健識局整理更多熱點新聞如下:
重磅政策
1、2022年公立醫院預算將縮減
3月24日,國傢衛健委官網發布《2022年部門預算》宣布,全年一般公共預算撥款總計將為180.59億元,同比增長5.97億元。其中,衛生健康支齣為96.06億元,占比53.19%。
健識局注意到,具體到公立醫院項目而言,撥給綜閤醫院、婦幼保健院,以及一部分專科醫院的款項均將減少,分彆為51.15億元、1.41億元和12億元,同比減少10.19%、23.88%和7.43%。
2、奧美拉唑等47個國采品種續約
3月23日,內濛古、四川等6省地發布《第一批和第三批國傢組織集中采購協議期滿藥品接續采購工作實施方案(徵求意見稿)》,宣布將對這兩批采購名單內協議期滿月藥品進行續約。
本次續約的産品總共有47個,包括奧美拉唑、阿托伐他汀、伊馬替尼、利培酮等産品。按照規則,6省內所有公立醫療機構均將參與,采購期為兩年。如果上一輪中選産品本次也納入瞭預選産品範圍,其約定采購量須達到該醫療機構約定采購量的50%,采購聯動國傢和各省最低價。
3、化療、透析等5種門診費可跨省結算
3月25日,國傢醫保局發文錶示,門診費用跨省結算覆蓋範圍正在不斷擴大。
圖源:國傢醫保局
截至2022年2月,全國總計有63個地區的826傢定點醫療機構啓動高血壓、糖尿病、惡性腫瘤門診放化療、尿毒癥透析、器官移植術後抗排異治療5種門診慢特病治療費用跨省結算試點。
國傢醫保局格外提到,今年以來門診慢特病相關治療費用跨省結算纍計4842人次,涉及醫療費用513.38萬元,基金支付365.27萬元,基金支付比例為71.2%。其中,2月份門診慢特病相關治療費用跨省直接結算2670人次,涉及醫療費用264.67萬元。
行業大事
1、原北京食藥監局黨組書記張誌寬被查
3月27日,中央紀檢委網站發布公告錶示,原北京市食品藥品監督管理局黨組書記、局長張誌寬因涉嫌嚴重違紀違法,目前正在接受紀律審查和監察調查。
公開資料顯示,張誌寬1975年參加工作,曾擔任過北京市工商行政管理局局長、北京市政府副秘書長等職務。起初,張誌寬並不在醫療係統內任職,直到2013年8月纔調任至北京市食品藥品監督管理局,並於2016年1月起不再擔任該局局長。
2、輝瑞新冠口服藥國內售價2300元一盒
3月25日,據浙江廣電集團經視新聞報道,首批輝瑞新冠口服藥Paxlovid已在浙江投入使用,售價為2300元/盒,並已納入醫保支付。
圖源:經視新聞
2022年2月12日,Paxlovid獲批在中國上市。3月21日,國傢醫保局發布《關於切實做好當前疫情防控醫療保障工作的通知》錶示,已經將這款産品納入到醫保支付的範圍中,並要求各醫療機構按企業和相關部門溝通一緻的價格采購,醫保部門按規定進行支付。
3、多地將新冠抗原檢測納入醫保
新冠抗原檢測試劑在國內獲批使用後,已有多地陸續將其納入醫保。健識局注意到,截至3月26日,河北、山海、浙江、湖北等19個地區均已發文錶示將新冠抗原檢測項目臨時納入醫保服務項目中,待疫情結束後自行廢止。
按照一般規則,自願檢測人員的檢測費用可通過個人醫保賬戶支付。此外,如果隻是進行新冠抗原檢測,公立醫療機構不得收取門診診查費或一般診療費。對於購買檢測試劑進行自測的人群,則不得收取新型冠狀病毒抗原檢測費用。
在價格上,大多省份要求公立醫療機構按照檢測項目+檢測試劑的方式收費,總費用不得超過15元/人次。也有個彆省份的價格低於這個標準,如湖南省要求總費用不得超過12元/人次。
4、白雲山等5傢企業因帶量采購失信被公示
3月24日,甘肅省醫保局發布《省帶量采購藥品中選企業失信行為處理結果》。廣州白雲山、山東鳳凰製藥等5傢企業因未履行承諾事項,“嚴重影響采購協議簽訂和中選藥品采購”而被公示處理。
《處理結果》顯示,在此前開展的廣東聯盟藥品帶量采購中,甘肅省醫保局要求中選企業與省藥采網應在2022年1月15日前建立起覆蓋全省103個區域的配送關係,而這5傢企業的8個中選産品未能按時履約。
新藥獲批
1、K藥治療子宮內膜癌適應癥在美獲批
3月21日,美國FDA發布公告錶示,批準默沙東的PD-1抑製劑Keytruda單藥用於治療晚期子宮內膜癌患者。
截至目前,K藥拿下的適應癥將近30項。2021年6月,默沙東在一場投資者會議上公布的數據顯示,K藥在超過30種癌癥中顯示齣活性。2月初,默沙東公布的2021年年報顯示,K藥全年收入達到171.86億美元,僅次於艾伯維的“修美樂”。
2、阿斯利康PD-L1Ⅲ期臨床失敗
3月24日,阿斯利康宣布PD-L1度伐利尤單抗聯閤放化療治療宮頸癌的一項Ⅲ期臨床試驗失敗。公司錶示,較之單純的放化療而言,這項試驗未能達到改善無進展生存期的主要終點。
健識局瞭解到,這項研究是一項隨機、多中心、雙盲的全球Ⅲ期臨床試驗,主要在美國等15個國傢的120個中心進行。試驗共計770名晚期宮頸癌患者參與。
度伐利尤單抗於2017年上市,並在2018年時獲中國國傢藥監局批準進入國內。截至目前,這款産品總共獲批瞭非小細胞肺癌、尿路上皮癌、頭頸部鱗狀細胞癌等多個適應癥。
3、武田ALK抑製劑在國內獲批上市
3月24日,國傢藥監局官網公示批準武田的ALK抑製劑布格替尼片brigatinib的上市申請。這是一款新一代強效選擇性酪氨酸激酶抑製劑,能夠作用於間變性淋巴瘤激酶分子變異,主要用於治療特定非小細胞肺癌患者。
此前,brigatinib已經在美國、加拿大和歐盟等國傢和地區獲批上市,曾被美國FDA授予突破性療法認定和孤兒藥資格認證。2021年1月,武田嚮中國國傢藥監局遞交瞭這款産品的上市申請。
分享鏈接
tag
相关新聞
有關東航墜機事故的一些疑問,權威迴應在這裏

失事飛機第二部黑匣子已找到

東方航空已正式啓動賠付工作,更多消息

剛剛通報:找到新的事故有關視頻

東航已正式啓動理賠工作
東航空難地點8公裏外找到新的有關視頻!周邊曾號召提供綫索

第二部黑匣子發現細節公布,東航已啓動理賠工作

昔日“央視一哥”60歲仍未婚,網友:他好慘

MU5735,未完成的告彆

連續15天日新增確診超韆例,疫情防控形勢仍然嚴峻復雜
緬甸曼德勒轄區一警局被襲擊

東航空難:第二部黑匣子數據存儲單元外觀完好 正式啓動賠付工作

太艱難!緬甸8個月爆發瞭兩韆餘次戰事

緬甸仰光破獲大型毒品案

以後在緬甸建房需要嚮警局報備

安樂死閤法、分娩鎮痛免費、創建麻醉治療科,他最想做的三件事

MU5735遇難者頭七祭 市民留言“在平行時空裏好好照顧自己”

公立醫院預算大幅縮減,後疫情時代如何應對效益下滑?

上海完成多個集中隔離收治點改建

貴州今年兩起煤礦事故緻22人死亡,國務院安委會實行掛牌督辦

強軍心路|你播綠瞭傢鄉,我守護你

老兵花甲之齡成為抗疫誌願者:“曾經當過兵,永遠是戰士!”

滾動更新|東航麵嚮遇難乘客傢屬開通理賠專綫

中國退役軍人·在希望的田野上|牟仕榮:脫貧攻堅擔使命,鄉村振興再齣發

延誤、物流信息更新緩慢……快遞不快瞭,咋迴事?

天府機場正式迎來夏鞦航季 旅客趕飛機要注意這些變化

新華視點丨還原東航墜機第二部黑匣子發現過程

被質疑“不夠悲傷”,墜機乘客傢屬遭遇網暴

有關東航墜機事故的一些疑問,權威迴應在這裏

東航空難“頭七”日 痛悼事故遇難者

這些文具孩子越喜歡,爸媽越要警惕:可能有毒

東航空難一綫救援人員:淤泥沒過膝蓋 雙手磨齣水泡

美國原住民人權活動傢被監禁46年 美司法體係被批種族歧視

給核酸檢測人員錶演節目,不如讓 Ta 們早點迴傢

又一傢醫院並入省級大三甲!成為新院區

默哀!MU5735航班上人員全部遇難

半月談:繼續追尋真相是對MU5735最好的告慰

在東北虎常齣沒的西伯利亞小鎮,居民要看好自己的狗

東航墜機頭七祭:沒有奇跡,願安息

截至3月26日24時新型冠狀病毒肺炎疫情最新情況








































