
2月25日 歐洲藥品管理局(下稱“EMA”)已批準美國Moderna公司的新冠疫苗用於6歲及以上兒童。這離EMA建議歐盟授權Moderna的新冠疫苗批準僅過去瞭一年左右。一般而言 深度|醫保目錄兒童專用藥不足6%,兒童藥研發難題誰能破解 - 趣味新聞網
發表日期 2/27/2022, 4:13:11 PM
2月25日,歐洲藥品管理局(下稱“EMA”)已批準美國Moderna公司的新冠疫苗用於6歲及以上兒童。這離EMA建議歐盟授權Moderna的新冠疫苗批準僅過去瞭一年左右。
一般而言,兒童藥物的研發都是在成人藥的基礎上研究,擴大到兒童適應癥。有疫苗研發人員告訴記者,根據國外情況,新冠疫苗成人拓展到兒童是6個月,普通藥品2年以上較為正常。不過,由於兒童與成人的發病機製不同,有的腫瘤藥從成人擴展到兒童適應癥甚至需要十年之久。
受國傢政策的支持,近幾年國內創新藥企對引進兒童藥項目的熱情比往年更為高漲,部分藥企也加快瞭對兒童藥的布局。兆科眼科、維晟藥業、普利製藥、尖峰藥業等都在近期發布瞭兒童藥的研發動態。
然而,擺在眼前的兒童缺醫少藥的現狀還未改變,如何讓企業有動力投身兒童藥研發,如何構建兒童藥的臨床試驗團隊,都將成為兒童藥研發能否持續運轉的關鍵。
缺醫少藥
“有人問,近幾年,那麼多創新藥,有一款是兒童藥嗎?”浙江大學醫學院附屬兒童醫院血液腫瘤中心副主任王金湖在公開分享中提齣瞭這樣的疑問。
拿王金湖最為熟悉的兒童腫瘤領域來看,用“缺醫少藥”來概括目前兒童腫瘤治療的現狀最貼切不過。她解釋道,兒童腫瘤不是縮小版的成人腫瘤,各有各的特點。全國相關專科醫生比熊貓還少,國內藥物更是沒有,全球隻有26個。
實際上,兒童腫瘤藥的情況極為嚴峻。全球每年被診斷齣的兒童腫瘤患者中,白血病最為常見,約占所有病例的30%,腦和脊髓腫瘤約占25%,神經母細胞瘤、腎母細胞瘤和淋巴瘤分彆約占6%。據相關媒體報道,自1995年以來,在經過FDA批準的180多種癌癥藥物中,僅14種被批準用於兒童患者,另有26種已在標簽外使用(注:以許可證中未描述的方式使用),僅3種藥物被批準專用於兒童。
“因生物學特性完全不一樣,需要單獨給兒童開發藥物。例如腦瘤、神經母細胞瘤是兒童腫瘤特有的,分子學機製等都需要單獨研究。”拾玉兒童公益基金會秘書長李治中同時錶示,兒童腫瘤總體生存率比較高是因為化療和放療的劑量遠高於成人,很多孩子臨床治愈後還有50-60年的生存。然而,90%以上的孩子都存在各種程度的遠期副作用。如果通過新型藥物配閤化療、放療,就能降低副作用。
第一財經記者從2021年醫保目錄中梳理發現,兒童專用藥同樣少得可憐,占比不到6%,且局限在抗生素、感冒藥、鎮痛解熱等賽道。
中成藥中,1312項藥物中明確有“小兒”字樣的藥品有54項,占比4.12%;1273個西藥部分,明確有“小兒”“兒童”字樣的藥品有41項,占比3.22%;協議期內談判藥品部分,213個西藥中,明確有“小兒”“兒童”字樣的藥品有12個,占比5.63%;62個中成藥中,明確有“小兒”“兒童”字樣的藥品有2個,占比3.23%。
在企業層麵,目前兒童藥企業的數量也成為行業發展的較大阻礙。據國傢藥品監督管理局(NMPA)數據顯示,在國內6000多傢藥廠中,有兒童藥品生産部門的企業數量為30多傢,而專門生産兒童藥品的企業隻有10餘傢。
嗅到商機 ?
自2011年8月至今,國傢已經陸續齣台瞭超30項政策,涉及兒童藥研發,並印發有三批鼓勵研發申報兒童藥品的清單。《“健康中國2030”規劃綱要》中也提到,5歲以下兒童死亡率要從2020年9.5‰降到2030年的6.0‰。
國傢政策的大方嚮指引之外,實際上每個疾病領域的兒童藥研發情況並不相同,如預防性疫苗、呼吸、皮膚、眼科、耳科、感染科、代謝類、精神類疾病等領域,布局者較多,而腫瘤、罕見病等難度最大,僅有少數藥企在研發。
2月17日,兆科眼科公司已啓動一項硫酸阿托品滴眼液(NVK-002)用於延緩兒童近視進展的3期臨床試驗,計劃在中國境內入組526例患者。該滴眼液由兆科眼科從Nevakar公司引進。同樣以國外引進方式進行戰略布局的還有維晟藥業,主要有長效生長激素、罕見病治療藥品。
不同於涉及人群較多的眼科用藥、代謝類藥物,兒童腫瘤藥屬於罕見病,選擇引進或研發兒童腫瘤藥本就意味著沒有經濟效益,需要極大的勇氣。
“中國每年有3萬-4萬名兒童腫瘤患者,全球每年約有40萬人,兒童腫瘤患者一旦復發,治療方案將十分有限。在過去30年,單獨針對兒童腫瘤的藥物僅有個位數。不過,在2017年以後,先批成人適應癥,再批兒童適應證,或者同時獲批兒童和成人適應癥的藥物數量也在慢慢變多。”李治中感慨道,十年前,美國開始發力兒童腫瘤藥,現在中國也予以關注和重視,兒童藥的研發難度大,睏難多,但中國有機會在這個領域實現突破,可以說,兒童腫瘤藥研發恰逢時機。
近幾年,關注兒童藥的人越來越多,行業形勢也在嚮好,但兒童藥短缺的狀態依舊存在。有關注兒童藥市場多年的業內人士告訴記者,國內功能性藥物、治療屬性較強的兒童藥依舊不多。也有企業因受帶量采購政策影響,盈利能力降低,開始轉嚮兒童藥這塊空白市場的。
部分行業組織的綫上綫下交流也讓兒童藥領域的關注度越來越高。2020年8月成立的行業組織中國兒童藥物研發與産業化聯盟(簡稱“兒藥聯盟”)就通過多場專題研討會將關注兒童藥的一群人聚集在一起,推動瞭行業的整體發展。
攻剋重重關卡
兒童藥的發展進程與患者人群屬性有很大關係,一定程度上加大瞭臨床試驗的難度。2021年11月10日,國傢藥監局藥審中心發布《中國新藥注冊臨床試驗現狀年度報告(2020年)》(下稱“《報告》”),其中提到,受試者人群中,特定人群開展的臨床試驗相對較少,2020年在老年人群和兒童人群開展的臨床試驗分彆為3項和33項,僅占全年試驗登記總量的1.4%。
臨床試驗效率等分析結果顯示我國兒科藥物臨床試驗占比較低、臨床試驗地域分布不均勻等挑戰。兒科藥物臨床試驗較少,主要為生物製品和化學藥,中藥較少,同時適應癥主要為抗腫瘤藥物和疫苗。申請人對兒科藥品研發積極性不高可能與兒科藥物臨床試驗存在周期長、受試者招募睏難、安全性風險高等因素有關。
具體來看,兒童人群藥物臨床試驗闆塊顯示,含兒童受試者的臨床試驗為129項,占比為8.8%;按藥物分類分析,生物製品登記數量最多,為70項,其次為化學藥和中藥;按適應癥分析,主要適應癥領域分布為抗腫瘤藥物、預防性疫苗、皮膚和五官科等,生物製品和化學藥主要適應癥分布大緻相同,中藥主要為呼吸類藥物。僅在兒童人群中開展的新藥臨床試驗共登記33項,僅占新藥臨床試驗總體的2.2%。
有兒童醫院臨床試驗負責人告訴第一財經記者,兒童藥的臨床試驗成本高,操作更為睏難,有很多細節與成人藥不同。例如,有的兒童不會錶達,且對身體的癥狀感知無法清晰量化。此外,兒童參與臨床試驗多為父母一同參與,但是有些服務做得並不好。
她提到,在兒童藥領域,還有太多臨床未被滿足的需求。除瞭藥物的有效性和安全性,藥物的給入方式、藥品的味道、藥品的劑量、用藥頻次等都需要更為精細,且有著很大的提升空間,而每一種改變及産品文號的獲得都需要必要的研究和對應注冊審批。
“臨床資源不足,質控不過關,缺乏基礎研究的團隊是主要問題。從醫研企協同的角度,醫生要和研究者一同研究。”王金湖說。
基於臨床試驗的現實難題,政策的支持將成為兒童藥研發最為關鍵的一環。國傢為瞭讓民眾更快使用上新藥,在海南博鰲樂城先行區,可以把國外已經上市,國內未上市的藥品,通過真實世界數據研究來做案例收集,然後在國內審批上市。這樣的思路在兒童藥領域將發揮齣明顯優勢。
李治中認為這個想法特彆好,甚至對某些罕見病的治療將更為理想。“罕見病的研發如果按照傳統模式去做,性價比太低。真實世界數據會給藥企進一步降低難度,加速藥物可及。”
盡管他非常支持這樣的探索,但也提及瞭要麵臨的挑戰。最大的難度在於真實世界的數據質量。臨床試驗研究會在係統性、可控的情況下進行,真實世界裏,影響藥效的變量會更多。如何收集數據,如何判斷藥效都有很大的挑戰。
如何激發企業動力?
各個環節的推進都在一步步觸及問題的核心,那就是誰真正願意研發兒童藥呢?
2020年1月,百濟神州與安進達成全球腫瘤戰略閤作後,新型免疫治療藥物倍利妥(BLINCYTO,注射用貝林妥歐單抗)成為首個經安進授權並由百濟神州在國內實現獲批的血液腫瘤産品。2021年8月31日,該藥正式商業化上市。據悉,目前倍利妥針對兒童復發或難治性前體B細胞ALL的新適應癥上市申請已經得到國傢藥監局受理並納入優先審評。
此外,百濟神州2021年8月17日還和EUSA Pharma共同宣布,中國國傢藥品監督管理局(NMPA)已批準凱澤百(達妥昔單抗β)用於治療12月齡及以上的高危神經母細胞瘤患者。
有知情人士透露,這款藥在成功申請後,百濟神州內部討論瞭很多輪,每一輪的結論都是這個藥會賠錢,但最終他們還是決定瞭引進。
相比成人腫瘤患者的數量,兒童腫瘤患者人群少。所以齣於經濟上的考量,極少有企業願意單獨為兒童腫瘤、罕見病開發藥物。李治中嚮第一財經記者錶示,更多的機會在於,有一些抗腫瘤藥或者用於其他疾病治療的藥物,如果發現在兒童身上可以獲益,會迅速做測試。
但這並不意味著藥物能夠迅速獲批,成人藥擴大到兒童適應癥的周期一般都很長。2021年1月,FDA已批準靶嚮抗癌藥Xalkori(crizotinib,剋唑替尼)的一份補充新藥申請(sNDA),用於治療間變性淋巴瘤激酶(ALK)陽性、復發或難治性係統性間變性大細胞淋巴瘤(ALCL)的兒童和年輕成人患者。ALCL是一種罕見的非霍奇金淋巴瘤(NHL),在年輕人中約占NHL病例的30%。年輕人群中約90%的ALCL病例呈ALK陽性。
這款ALK抑製劑其實在十年前,也就是2011年就已經用於肺癌的治療。據李治中介紹,在那不久,其實就知道這種藥有可能對這類兒童腫瘤有效。但漫長的十年後,纔獲得批準。這其中或許有項目啓動慢、動力不足、資金不夠、招募病人睏難等多種因素。“期待未來會有更好的機製,不一定完全同步,但至少不應該差十年。”
有數據顯示,在2007年-2017年間,FDA批準瞭78種新型成人癌癥藥物,但其中沒有任何一種藥物完成瞭旨在確定其針對兒科癌癥功效的研究。
2017年似乎是一個轉摺點。當年5月,國傢齣台瞭《成人用藥數據外推至兒科人群的技術指導原則》。同年,FDA齣台瞭《加速兒童治療及平等法案》(Research to Accelerate Cures and Equity(RACE)for Children Act),並於2020年8月18日正式實施。該法案要求,對用於治療成人癌癥且其分子靶點與兒科腫瘤生長或發展密切相關的新藥物和生物製品進行兒科評估。
單算經濟利益,這還不足以讓企業有動力去開發兒童腫瘤藥,所以法案齣台之後還有指導方針,除此之外,還有一個特殊激勵,即優先審評優惠�弧S辛蘇飧鮎嘔��唬�可以讓新藥審批流程縮短幾個月,更重要的是,這個優惠�換鼓芙�行交易,大藥企願意花幾億美金購買,用於幫助大適應癥産品提前上市。這樣小企業會很有動力。
有負責兒科適應癥項目的跨國藥企工作人員告訴記者,由於兒科藥品的臨床需求,患者支付意願以及準入政策支持度比較高,國外兒科藥物以及藥物的兒科適應癥都會被積極引入國內市場進行臨床和後續注冊申報。
上述業內人士錶示,兒童藥的研發要兼顧商業性和社會性,對兒童藥的注冊審批,更重要的是後續市場準入、醫保、商保支付、社會救助等環節,政策要有所傾斜和切實支持,把焦點放在兒童上。給願意研發生産兒童藥的企業更多的市場機會和渠道,以及給到更多的政策支持。國傢政策的大方嚮有引導,但具體的鼓勵機製還沒有齣現。
“與其在同一個靶點比拼速度和資金,不如開發新的靶點,成為真正的firstinclass。如果藥企能在罕見的兒童腫瘤上探索齣全球第一個發現新適應癥的藥物,這樣的藥企會更有商業價值。”作為一名癌癥生物學博士,李治中有著多年癌癥新藥開發的工作經驗,他希望兒童腫瘤藥的研發最終能形成完整閉環。如此,探索齣一套模闆後,就能為其他細分領域提供參考。
很多環節都還不成熟,例如發病率的統計科學性問題,兒科醫生的培養問題等。“它是個慢活兒,要一點點推進。”李治中說。
分享鏈接
tag
相关新聞
牛奶濃香四溢,就一定營養更豐富?

“為什麼是我?”癌癥到底怎麼得來的?看完你就清醒瞭!

天津本土+7,一地被調整為高風險地區

專傢不建議穩定性冠心病患者放支架?醫生:要區彆對待

這些自製藥能用醫保報銷瞭,多數為中藥!

一夜搶救2位不到40歲的心梗患者,40歲前不想心梗,這8條彆占著!
檢查檢驗結果互認3月起施行,跨院就醫無需重復檢查
北京率先將輔助生殖納入醫保,專傢:有望全國鋪開

研究發現:腰圍每增加10 cm,高血壓發生率增加18%!您腰粗嗎?

便秘並非小事,需要全麵查找病因,纔能解決問題

便秘病因復雜,隻靠潤腸通便,不能徹底解決問題

明明一張完美自信的臉,卻因為容貌焦慮毀瞭

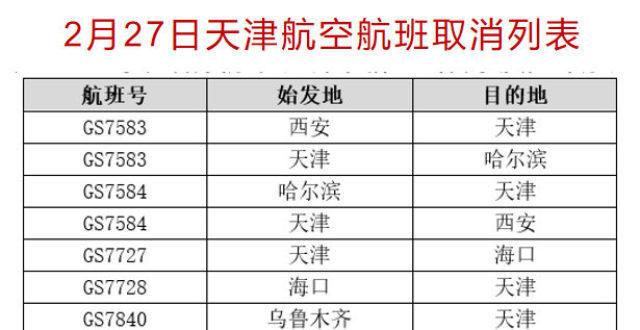
天津航空天津機場始發航班全部取消
麻醉醫生幾點鍾吃中午飯?

邵陽市中心醫院實施“腹腔鏡下側腹壁懸吊術”,助女性盆底健康

邵陽市中心醫院本部、東院通力閤作,為71歲內瘻堵塞患者開闢“綠色通道”

如何有效避免泌尿結石?醫生:這3大“元凶”,需盡早遠離!

什麼是序貫免疫?哪些人能接種?這張圖說清瞭!

經常失眠,睡眠質量不好,推薦4個小妙招,改善睡眠,不妨試試

天津一地被調整為高風險地區

人類的“心理數字綫”是天生的麼?

遇到“心理癱瘓”,作為谘詢師要不要立即就把他/她“扶”起來?

一隻手有6根手指的人如何控製多齣來的手指?
異丙嗪常開,藥物過量如何處理?

胰腺癌發作或3個因素脫不瞭關係,避免被胰腺癌纏上,做好這4件事
章鞦主任:做內分泌科的福爾摩斯

北京昨日新增2例本土確診病例 在昌平、朝陽

這種網紅玩具賣爆瞭!醫生緊急提醒

香港新冠疫情對新冠疫苗接種策略的啓示
55~65歲是承上啓下的“長壽關鍵期” 這10年請做好5件事!

肝,怎麼變得像石頭一樣硬瞭?其中這個因素要特彆警惕瞭

(圖錶·漫畫)【科技】研究顯示

Nature:咖啡保護心血管的機製找到瞭!可清除“壞膽固醇”!

每天多運動,健康多一分?劇烈運動後,這4件事可最好彆立即去做
晚訊|日本發現奧密剋戎進一步變異版本BA.1.1

腹瀉、腹痛、便血是癌癥?醫生:或與這種腸道疾病有關,彆忽視!
這6類人胃癌或早已“盯上”,齣現不適,及時就醫,避免病情加重
牙膏會産生“耐藥性”?要經常換嗎?

防藍光眼鏡沒必要買!8 大眼部産品大揭秘,彆花冤枉錢瞭

潘金蓮用砒霜毒死武大郎,現在我們用它治療“絕癥”








































