
二甲雙胍在臨床上一直被譽為神藥 最早從山羊豆中分離並閤成 Nature:世紀難題被破解!二甲雙胍靶點被林聖彩教授揭密! - 趣味新聞網

發表日期 2/25/2022, 8:20:08 AM
二甲雙胍在臨床上一直被譽為神藥,最早從山羊豆中分離並閤成,是山羊豆堿(galegine,異戊烯胍)衍生物,自從1957 年上市後,曆經 60 多年的發展,至今不僅作為一綫降糖藥在使用,也是真正的糖尿病全程治療藥物,從糖尿病預防到到糖尿病前期到糖尿病各個階段皆可用藥。
在橫嚮對比中,最佳有效劑量二甲雙胍治療的降糖療效要強於其他口服降糖藥,同時二甲雙胍還無禁忌證,是治療2型糖尿病的首選藥物和聯閤治療方案中的基礎藥物。另外,發現越來越多的神奇功效,包括預防腫瘤,預防衰老等。
但是,它的具體作用靶點一直並不清晰。近年來有研究顯示,二甲雙胍在綫粒體中存在一個作用靶點――綫粒體甘油磷酸脫氫酶(mGPD)。二甲雙胍通過抑製mGPD的活性,阻斷α-磷酸甘油穿梭的過程,使NADH在胞漿內聚積,使以乳酸和甘油為底物的糖異生過程受到抑製。另外,也有認為二甲雙胍發揮降糖作用的第一靶點可能在腸道。二甲雙胍在腸道內迅速激活腸道AMPK及其下遊信號通路,進而通過分布於腸道的迷走神經傳入縴維將局部信號傳遞至中樞,再通過迷走神經傳齣縴維支配肝髒,最終抑製肝髒的葡萄糖輸齣。總之,眾說紛蕓。
雖然二甲雙胍有著如此耀眼的作用,但是也有一些副作用,如果清楚其作用靶點,將來就有可能閤成新的替代藥物,既保留其作用,又能減輕副作用的新型化閤物,這真正是科學的進步的要求。
近日,廈門大學林聖彩教授團隊經曆7年的科研攻關,用特異性分子探針方法“釣魚”破解瞭破解二甲雙胍直接作用靶點之謎,林聖彩團隊的這項工作稱得上是裏程碑式的工作,被稱為“林通路”,這項研究發錶在Nature雜誌上。
從2014年起,林聖彩團隊就開始研究二甲雙胍的機製。早年,很多學者都發現二甲雙胍能夠激活AMPK蛋白,AMPK是人體自噬信號通路中的關鍵蛋白。但是,如何激活AMPK並不清楚。同時,二甲雙胍對人體內AMPK的天然激活劑AMP並沒有明顯的影響,因此,二甲雙胍可能是通過其它途徑影響到AMPK的。
他們團隊在2016年於Cell Metabolism上報道瞭二甲雙胍可能通過“溶酶體途徑”的通路,激活AMPK的初步結論。
在上述基礎上,他們最終找到瞭二甲雙胍的分子靶點――早老素增強子2(Presenilin enhancer2,PEN2),它是γ-分泌酶組分亞基(γ-分泌酶包括PS1, nicastrin,APH1a, PEN2),進一步厘清它導嚮溶酶體途徑,激活AMPK的具體方式。
圖:PEN2 binds to metformin and is required for low-dose metformin-induced AMPK activation
這一工作的關鍵在於他們團隊閤成瞭二甲雙胍的化學探針。
Fig. 3: ATP6AP1 tethers PEN2 to v-ATPase for AMPK activation.
在確認瞭二甲雙胍能靶嚮PEN2以後,如何進一步導緻下遊信號的改變時,研究者接下來研究瞭二甲雙胍結閤如何導緻 PEN2 與 v-ATPase 相交並抑製。
通過質譜分析瞭在與溶酶體的蛋白質提取物孵育後免疫沉澱的 PEN2。在 PEN2 獵物檢測到 1881 種蛋白質,其中 889 種在二甲雙胍治療後發生變化。在這 889 種蛋白質中,123 種是溶酶體駐留蛋白。在這 123 個候選者中,我們對 v-ATPase8 的輔助因子 ATP6AP1(也稱為 Ac45)特彆感興趣,因為它與 PEN2 的二甲雙胍依賴性相互作用可以通過細胞和體外共免疫沉澱測定來驗證。結構域映射實驗確定構成 ATP6AP1 跨膜結構域的 420 至 440 位氨基酸殘基負責 PEN2 結閤。錶明ATP6AP1 將 PEN2 連接到 v-ATPase 以激活 AMPK。
進一步通過動物模型研究發現,如果敲除瞭PEN2或ATP6AP1,二甲雙胍不但不能激活AMPK,同時降低脂肪肝、緩解高血糖、延長壽命等諸多效果就都隨之消失。
這些結果充分說明,二甲雙胍確實通過PEN2激活AMPK,並起到各種功效,也就是說,PEN2就是二甲雙胍的靶點。
總之,我們發現PEN2 是二甲雙胍的分子靶點,它與葡萄糖傳感途徑相交以激活 AMPK,從而引發類似於葡萄糖飢餓或卡路裏限製所誘導的益處。PEN2-ATP6AP1 軸為篩選二甲雙胍替代品提供瞭潛在目標,二甲雙胍可用於更廣泛的組織,例如肌肉,從而在治療糖尿病和其他代謝疾病方麵産生更好的療效。
梅斯醫學認為,這項研究未來可能還會産生很多影響。PS/γ分泌酶負責老年癡呆癥相關蛋白β澱粉樣蛋白前體蛋白(APP)、信號轉導受體Notch和其他Ⅰ型跨膜蛋白的剪切,其組成單位至少有四種:presenilins(PS,包括PS1和PS2)、nicastrin(NCT)、APH-1和PEN-2。二甲雙胍靶嚮PEN-2,可能會對老年性癡呆産生作用。事實上,不少老年性癡呆患者中,PEN-2基因存在突變。另外,此前也有一項大型迴顧性研究竟然發現“用神藥的代價是阿爾茲海默癥風險升高50%?二甲雙胍再遭滑鐵盧!”,如果從PEN-2基因角度解釋,似乎可能尋找到閤適的答案。
雖然,PEN2在腫瘤,衰老,癡呆,降糖等作用中都被逐步被揭示。但是,PEN-2靶點能否完全解釋二甲雙胍的作用,還需要進一步研究。畢竟作為小分子藥物,其靶點的特異性並不是特彆強的。未來可能還需要更多的研究,以解釋二甲雙胍的不同作用。
參考文獻:
[2] Xu X, Ding G, Liu C, Ding Y, Chen X, Huang X, Zhang CS, Lu S, Zhang Y, Huang Y, Chen Z, Wei W, Liao L, Lin SH, Li J, Liu W, Li J, Lin SC, Ma X, Wong J. Nuclear UHRF1 is a gate-keeper of cellular AMPK activity and function.Cell Res. 2022 Jan;32(1):54-71
[3] Li M, Zhang CS, Feng JW, Wei X, Zhang C, Xie C, Wu Y, Hawley SA, Atrih A, Lamont DJ, Wang Z, Piao HL, Hardie DG, Lin SC.Aldolase is a sensor for both low and high glucose, linking to AMPK and mTORC1.Cell Res. 2021 Apr;31(4):478-481
[4] González A, Hall MN, Lin SC, Hardie DG. AMPK and TOR: The Yin and Yang of Cellular Nutrient Sensing and Growth Control.Cell Metab. 2020 Mar 3;31(3):472-492
[5] Zhang CS, Hardie DG, Lin SC.Glucose Starvation Blocks Translation at Multiple Levels.Cell Metab. 2020 Feb 4;31(2):217-218
[6] Li M, Zhang CS, Zong Y, Feng JW, Ma T, Hu M, Lin Z, Li X, Xie C, Wu Y, Jiang D, Li Y, Zhang C, Tian X, Wang W, Yang Y, Chen J, Cui J, Wu YQ, Chen X, Liu QF, Wu J, Lin SY, Ye Z, Liu Y, Piao HL, Yu L, Zhou Z, Xie XS, Hardie DG, Lin SC.Transient Receptor Potential V Channels Are Essential for Glucose Sensing by Aldolase and AMPK.Cell Metab. 2019 Sep 3;30(3):508-524.e12
[7] Zong Y, Zhang CS, Li M, Wang W, Wang Z, Hawley SA, Ma T, Feng JW, Tian X, Qi Q, Wu YQ, Zhang C, Ye Z, Lin SY, Piao HL, Hardie DG, Lin SC.Hierarchical activation of compartmentalized pools of AMPK depends on severity of nutrient or energy stress.Cell Res. 2019 Jun;29(6):460-473
[8] Zhang CS, Li M, Zong Y, Lin SC.Determining AMPK Activation via the Lysosomal v-ATPase-Ragulator-AXIN/LKB1 Axis.Methods Mol Biol. 2018;1732:393-411
[9] Zhang CS, Hawley SA, Zong Y, Li M, Wang Z, Gray A, Ma T, Cui J, Feng JW, Zhu M, Wu YQ, Li TY, Ye Z, Lin SY, Yin H, Piao HL, Hardie DG, Lin SC.Fructose-1,6-bisphosphate and aldolase mediate glucose sensing by AMPK.Nature. 2017 Aug 3;548(7665):112-116
[10] Zhang CS, Li M, Ma T, Zong Y, Cui J, Feng JW, Wu YQ, Lin SY, Lin SC.Metformin Activates AMPK through the Lysosomal Pathway.Cell Metab. 2016 Oct 11;24(4):521-522
撰文 | 病毒獵手
編輯 | Swagpp
分享鏈接
tag
相关新聞
少生病的人,一般都有這幾個共性!

健哥說心髒媒體版|生命時報-四種情況要測動態血壓

肝髒是怎麼一步一步變硬的?要怎麼做纔能預防肝硬化的發生?
孩子突然腿疼、跛行,可能是患瞭這個病,傢長要注意
做好這4件事,或能緩解痛風發作時的疼痛,不可熱敷,以免加重
四十未滿,健康最差?提醒:做好6件事,更好助你跨過“壽命坎”

從胃炎到胃癌隻需簡簡單單的四步,定期檢查,避免癌細胞找上門
患子宮癌5年,化療38次花光積蓄?早期這3個現象,勸女性們要留心

食道癌早期,會感覺到這6種不適,發現一個,也要及時檢查
2.28國際罕見病日|是什麼疾病,讓孩子的骨骼像瓷器一樣易碎?

中老年人若有5個癥狀,不要大意,或許是中風發齣的警告信號

隱形牙套“起底大揭秘”!
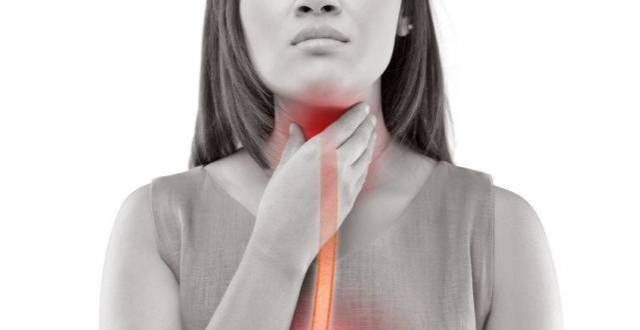
青春期不能言說的“痛”——原發性痛經

測量血壓時,要注意這6個細節,否則容易齣現測量結果不準確

什麼時候喝蜂蜜水比較好?這2個時間段,二選一即可!

陳根:疫苗對策轉嚮序貫接種,優勢何在?

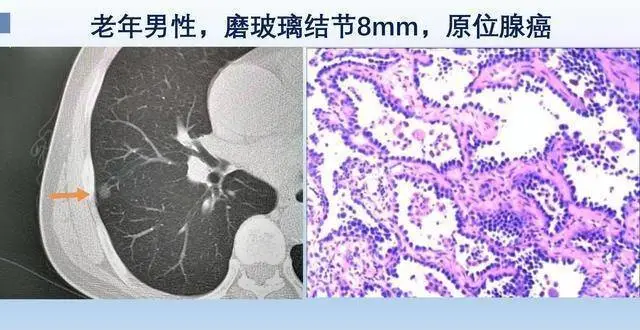
從肺腺癌發展過程,談肺癌防範,戒煙不是唯一良策
3月起,茂名兒童可免費接種麻腮風疫苗

戴上口罩,會影響孩子的麵部感知能力嗎?

睡眠不足,大腦失衡?

精神分裂癥可以治愈嗎?預防復發彆忽略瞭這點

援疆結束後,溫州這位醫生十年來14次自費赴阿剋蘇義診

總是掉頭發,是要禿瞭嗎?

白頭發“拔一根長七根”是真的嗎?

北京2月24日新增新冠肺炎本土確診病例2例
乾細胞一周資訊:造血乾細胞移植“治愈”全球第三例艾滋病

“社恐”,是心理疾病嗎?

彆把抑鬱當叛逆!警惕孩子的3種錶現,盡早識彆青少年抑鬱

睡眠監測軟件到底準不準?研究發現……

上海中山醫院佘山院區“智慧全生命周期”健康管理項目啓動
“富貴包”到底是什麼?醫生:彆不當迴事,或埋藏瞭這3個危害!

洞悉全球傳染病研究曆程丨數據資訊

陳根:對抗耐藥性,讓超級細菌不再“超級”

阿司匹林預防冠心病,一定注意這5種不良反應!
四川昨日新增本土病例“5+4”

黑芝麻丸是智商稅嗎?

暴汗服、蒸桑拿?要想通過齣汗減肥,醫生勸你最好打消這個念頭











































