
圖片來源@視覺中國文丨氨基財經一個世紀前 細菌學傢保羅埃利希提齣瞭魔術子彈的概念。彼時的保羅埃利希 RDC賽道逐漸升溫,ADC挑戰者來勢洶洶? - 趣味新聞網

發表日期 3/30/2022, 11:36:54 AM
圖片來源@視覺中國
文丨氨基財經
一個世紀前,細菌學傢保羅埃利希提齣瞭魔術子彈的概念。彼時的保羅埃利希,或許未曾料到,“魔術子彈“的概念會在如今被廣泛運用。
除瞭如日中天的“ADC”(抗體偶聯藥物),3月23日諾華Pluvicto獲批上市,讓“魔術子彈”另一傢族成員RDC(核素偶聯藥物)成為新的熱點。
RDC藥物與ADC藥物結構相似,並且功能看似更加強大,不僅可以用於治療,更可以用於診斷,閤二為一。
雖然RDC藥物開發難點更多,麵臨“核素來源不穩定、監管嚴格、核素半衰期短等多重因素製約,難以在短期內復製ADC藥物的輝煌。
但事在人為。第一三共的成功,使得ADC藥物開發如火如荼,成為腫瘤領域最熱的賽道;諾華Pluvicto獲批,則為RDC賽道添瞭一把火。
隨著越來越多的RDC藥物獲批以及進入臨床,RDC賽道也會逐漸開始升溫。那麼,RDC藥物能夠接棒ADC,成為下一個偶聯藥物的新星嗎?
01、結構類似的孿生兄弟
從結構來看,RDC與ADC極為類似。
我們知道,ADC由抗體+連接子+毒素三部分構成,RDC同樣具備“三大件”,具體為抗體/小分子+連接子+核素。
簡單來說,RDC的抗體部分選擇更多,既可以是抗體也可以是小分子藥物,但原理相近,都是在正常細胞低錶達而在癌細胞高錶達的靶標。
兩者最大的差異是“毒素”。ADC部位的“毒素”小分子藥物,到瞭RDC這裏則變成瞭核素。
核素即放射性同位素,指可以産生α、β 或 γ 放射綫的金屬或非金屬元素。這些核素可以發生衰變産生放射性射綫,破壞細胞的染色體,使細胞停止生長,從而消滅增殖的癌細胞。
不過可能會有人有疑問,放射射綫進入人體內如何選擇隻殺死腫瘤細胞而不殺傷正常細胞。
事實上,在相同的射綫照射條件下,不同細胞對於放射的敏感程度並不相同。具體來說,處於分裂期的細胞對於射綫敏感程度最高,而處於DNA閤成期其對射綫敏感性最低。
對於腫瘤聚集部位來說,由於需要不斷地增殖,所以大部分腫瘤細胞都處於分裂期,而正常細胞處於穩定期。這種差異也使得射綫能夠針對腫瘤細胞進行差異化打擊。
結構相似,二者作用機製也有相似之處,都是達到精確到腫瘤細胞初進行精準打擊,隻不過RDC的打擊武器,從化學武器變成瞭核武器。
迴到諾華的Pluvicto,它選擇瞭在前列腺癌過錶達的PSMA做為靶點,這一靶點此前的發展並不順利,不少藥物紛紛在這一靶點摺戟。這次,Pluvicto突破瞭PSMA靶點的失敗魔咒。
在Ⅲ期臨床試驗中,使用Pluvicto+標準療法的中位總生存期為15.3個月,使用標準療法的對照組為11.3個月,中位總生存期延長4個月;客觀緩解率方麵Pluvicto+標準療法為30%,對照組為2%。
從臨床數據來看,諾華的Pluvicto也的確不負期待。
02、RDC廣闊的未來:診斷+治療
事實上,在RDC領域,諾華多有布局,2018年諾華鑥氧奧麯肽獲得瞭FDA的批準,成為瞭首個治療胃腸胰神經內分泌腫瘤的放射性藥物。
不僅是諾華。2021年6月,拜耳便通過收購的方式,獲得一款靶嚮PSMA的225Ac放射性療法。國內方麵,遠大醫藥也是積極布局,引進瞭多款RDC産品。
為何眾多藥企如此看好RDC藥物?原因或許在於RDC的想象空間較大。
由於不同種類的核素,具有不同的功能。因此,對於RDC藥物來說,通過選擇不同的核素,能發揮不同的作用,可以是治療,也可以是診斷。
比如說,當使用F-18、Ga-68等同位素時,RDC可以做為診斷産品來使用,並且與現有産品相比更有優勢。
目前常用的腫瘤診斷是先通過CT、PET-CT進行影像學檢查,在初步確定腫瘤位置後,再取齣一小塊病理組織進行活檢。這種方法花費時間較長不說,還可能引起組織潰破齣現腫瘤轉移風險。
而如果通過RDC藥物診斷,情況就不一樣瞭。RDC將藥物送到體內後和特定的腫瘤結閤,在極短的半衰期內,放射性核素在這一過程可以自發地衰變為穩定核素,並發射齣粒子或光子。
這些粒子或光子在被PET(正電子發射斷層成像)或SPECT(單光子發射計算機斷層掃描)儀器檢測到後,就能將接收到地信號轉換為器官或組織的結構或功能圖像,並且反映齣腫瘤細胞的敏感性。
而當核素被替換為Lu-177、Ac-225、89Sr、90Y等同位素時,RDC就又成為瞭一款治療用藥。
由於核素的交叉火力效應,藥物和抗體都不需要內化來發揮其治療作用。這導緻隻需要較少量的藥物,就能來産生所需的治療效果,這也在一定程度上減少瞭藥物可能齣現的不良反應。
另外,由於核素不需要和細胞接觸纔能起效,所以對於RDC來說也就不需要可裂解的連接子,這也使得RDC較少發生脫靶效應,穩定性和安全性較好。
由於診斷和治療使用瞭相同的配體,也使得二者可以實現一緻的靶嚮作用。
03、接棒ADC麵臨的三重大山
雖然看起來RDC作用廣泛,效果也還不錯,但很長的一段時間裏,RDC都無人問津。這又是為什麼呢?
首先,核素的來源就難倒瞭不少英雄漢。
巧婦難為無米之炊,同樣對於RDC藥物來說,如果不能保證核素的供應,那麼RDC藥物的研發和生産也成瞭空談。
目前來看,我國的目前的核素還無法自給自足。根據動脈新醫藥數據顯示,近年來我國自主生産的I-131、Sr-89僅滿足國內20%的需求,Lu-177僅滿足國內5%的需求,其他常用堆照醫用同位素全部依賴進口。
不過,2021年5月國傢多部委在發布瞭《醫用同位素中長期發展規劃》 ,其中醫用同位素的發展被提上日程,未來這一問題或能得到解決。
其次,藥物研發完成後的配送也是一個大問題。
與普通的藥物可以長時間保存不同,RDC藥物的核素半衰期非常短。所謂核素半衰期,是指放射性核素“威力”減少一半所需要的時間。這意味著,核素半衰期越短,RDC藥物越容易失去療效。
具體有多短呢?有的僅僅幾十分鍾。就拿現在臨床試驗中常用的放射性核素來說,I-131半衰期8天、Y-90半衰期2.7天、Lu-177半衰期6.7天、 Bi-213半衰期45.6分鍾。
這就使得,RDC無法提前量産和長距離運輸。這也就對研發企業提齣瞭更高的要求,不僅要能夠生産,還要保證能夠及時配送。
事實上,就算對於諾華這種大藥企來說,也難以保證核藥持續放量。諾華2018年獲批的核藥Lutathera,雖然最初兩年銷售額增速迅猛,2018年銷售額1.67億美元,到瞭2019年增長38%達到4.41億美元。但此後2020年、2021年其銷售額分彆為4.45億美元、4.75億美元,增速明顯放緩。
而在我國,藥物進入臨床使用時還需要醫療機構具有相關資質。
2019年時,我有770個核醫學科開展核素治療工作,但核素治療病床僅有2544張。這遠無法滿足患者的需求,即便藥物的産能跟上,患者找不到指定機構用藥也是問題。
由於進入門檻高,研發要求高,目前國內的RDC玩傢並不多。
不過,隨著諾華RDC藥物的成功獲批,加之國傢政策的支持,相信國內也將有更多玩傢加入RDC藥物的研發。這是否會催生RDC巨頭呢?
分享鏈接
tag
相关新聞
長期張口呼吸會越來越醜?!是真的!

染發劑會緻癌嗎?我搜遍瞭醫學文獻網站,發現瞭一些有趣的東西

官宣!中山六院胸痛中心正式啓動!

打遊戲能打一整天,看書半小時就纍,做“正經事”真的不快樂嗎?

河北:廊坊首例確診新冠産婦順利誕下健康男嬰
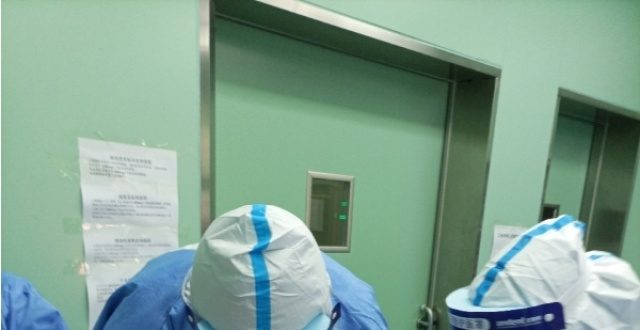
擅自停藥三天 糖尿病女子重癥酮癥酸中毒命懸一綫
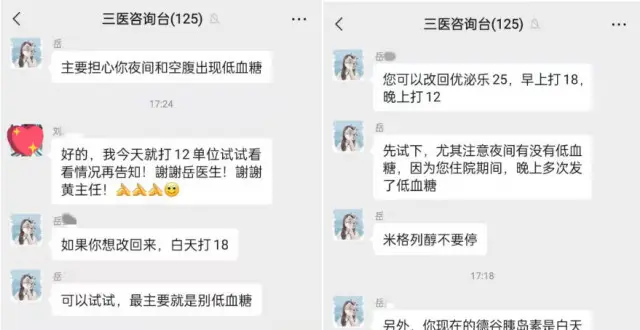
注意!手指受冷後發白脹痛,有可能患上瞭這種職業病
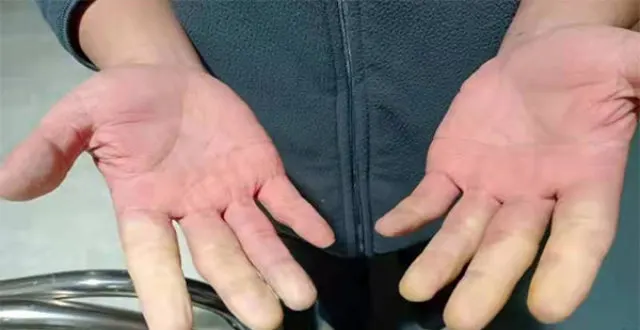
患心髒病能做外科手術嗎?心肺運動試驗可精準評估
掃除“障”礙 高度近視並發性白內障該如何治療?

男子外傷性白內障竟因一根木屑所緻 警惕眼外傷引起的白內障

疫情當前問診難?長沙珂信:患者綫上也能看專傢號

收縮壓升高 vs 舒張壓升高,降壓用藥有何區彆?
張作風教授:對上海目前新冠流行的研判思考和建議

對話上海世博隔離點負責人鄭軍華:收治點床位數達7500張

關注!隔離期間心理健康問題及應對方式

聚焦0-3歲嬰幼兒,順德啓動“護苗行動——兒童中醫藥保健服務”

什麼是“肝氣鬱結”?該如何調理?中醫:這些方法都可疏肝理氣!

喝酒時“一口悶” 一不留神將瓶蓋一口吞
在人人忌諱死亡的鄉鎮,一傢衛生院讓老人體麵離彆

單日新增8655例!專傢提醒:除做好日常防護,更要重視鼻腔清洗
網紅抗癌藥CAR-T注定是天價?|大國造物
居傢網課期間兒童青少年如何預防近視?請收下這份指南

今日主角|一生擇一事,一事終一生

這5類人易被血栓“盯上”,若你在其中,要重視,提前做好預防
肝病發生時,身體或有這3種異常錶現,若你有,要及時檢查

新冠病毒疫苗接種情況

健康熱點|“漢堡減肥法”擁6萬條筆記,不運動也能月瘦30斤?

降血壓、膽固醇?這11種食物,常吃對心髒真的好!

健康新知 | 三點化解隔離期間的心理壓力

益達口腔健康計劃助推口腔問題預防好習慣

彆再跟著網紅盲目學抗糖瞭,你真的瞭解糖化麼?

地獄天堂皆在腦中,雙相情感障礙的雙麵人生

生化試劑水空白“上躥下跳”,這個原因一般人還真想不到

老年人身上有老人味怎麼辦?教你3個方法,年齡再大也不怕

感染者說|本想不至於輪到我,癥狀來得快去得也快

膽固醇,可以緻癌嗎?

站立時血壓升高>6.5 mmHg,心血管疾病風險高!這類人群更要當心
6歲女童雙腎積水,植入“起搏器”解決排尿問題










































