��藥明康德內容團隊編輯癌癥是最受關注的疾病領域之一。從疾病負擔角度看 癌癥每年造成近1000萬例死亡 深度盤點:2022年抗癌藥物研發動態全景(1-4月) - 趣味新聞網

發表日期 5/9/2022, 7:37:47 AM
��藥明康德內容團隊編輯
癌癥是最受關注的疾病領域之一。從疾病負擔角度看, 癌癥每年造成近1000萬例死亡,占全球死亡總數的近六分之一,有著巨大的未竟醫療需求。 而從每年的新藥獲批角度看,在過去五年裏,FDA批準的創新療法中,數量最多的也是治療癌癥的藥物,占每年獲批新藥的近三成。在今天的這篇文章裏,藥明康德內容團隊將結閤 今年1-4月的新藥獲批、監管更新、以及臨床進展,為各位讀者送上最新的抗癌藥物研發動態。
內容概要
共有 5款 全新抗癌療法首次獲批
共有 4款 創新抗癌療法獲FDA突破性療法資格,其中3款尚未獲批
共有 7款 創新抗癌療法獲FDA優先審評資格,其中2款尚未獲批
共有 17款 抗癌療法在統計區間內獲得積極3期臨床試驗結果,或遞交上市申請
海外共有 10傢 抗癌新銳公司獲得5000萬美元及以上的融資
取得進展的研發新聞中,最常見的靶點依然為 PD-1 ,其次為 HER2
取得進展的研發新聞中, 小分子藥物、單剋隆抗體、抗體偶聯藥物 相關的新聞數並列第一
A輪融資不低於5000萬美元的海外新銳公司中,有30%關注 創新細胞與基因療法 ,20%關注 分子膠蛋白降解療法 ,20%關注 新型免疫療法
注:統計區間為2022年1月-4月
獲批新藥
今年一到四月間,美國FDA一共批準瞭十二款新藥,其中四款用於癌癥治療,占比三分之一,與曆史數據接近。 這四款新藥中不乏亮點,包含瞭 首款獲批的TCR療法和首款獲批的LAG-3抗體。 同期,中國NMPA也批準瞭多款創新抗癌療法,其中來自復宏漢霖的抗PD-1單抗尚未在全球其它國傢和地區獲批。

Kimmtrak(tebentafusp-tebn)
Immunocore
Kimmtrak在今年一月獲批,治療特定的葡萄膜黑色素瘤。作為一款創新的雙特異性蛋白,Kimmtrak由兩部分融閤而成:一端是具有高親和力的可溶性T細胞受體,另一端是抗CD3的免疫效應結構域。這款療法能特異性地靶嚮gp100,一種在黑色素細胞和黑色素瘤中錶達的抗原。 這項批準創下瞭多個第一:它是FDA批準的首款治療不可切除或轉移性葡萄膜黑色素瘤的療法。它同樣是首款獲得監管批準的T細胞受體(TCR)療法,以及首款獲FDA批準的治療實體腫瘤的雙特異性T細胞接頭。

Vonjo(pacritinib)
CTI BioPharma
Vonjo在今年二月獲批,治療伴有嚴重血小闆減少癥的骨髓縴維化(myelofibrosis)患者,這是骨髓癌的一種類型。 Pacritinib是一款新型的口服激酶抑製劑,能特異性抑製JAK2、IRAK1和CSF1R。因為它不針對JAK1,因此可以避免抑製JAK1帶來的潛在副作用。

Opdualag (nivolumab 與 relatlimab)
百時美施貴寶
今年三月獲批的“first-in-class”療法Opdualag由固定劑量的抗LAG-3抗體藥物relatlimab與抗PD-1抗體Opdivo(nivolumab)聯閤組成,治療罹患不可切除或轉移性黑色素瘤的成人和兒童(12歲及以上)患者。 值得一提的是,relatlimab是美國FDA批準的首款LAG -3抗體,也是近十年來針對全新免疫檢查點獲批的首款創新癌癥免疫療法。 臨床數據顯示,接受nivolumab單藥治療的初治轉移性或不可切除的黑色素瘤患者,其中位無進展生存期為4.6個月(95% CI: 3.4-5.6)。而接受組閤療法的患者中位PFS顯著延長,為10.1個月(95% CI: 6.4-15.7)。這是在轉移性黑色素瘤中,首個相對於抗PD-1抗體單藥治療還能具有統計學獲益的治療方案。

Pluvicto(lutetium Lu 177 vipivotide tetraxetan)
諾華
同樣是在今年三月,諾華的靶嚮放射性配體療法Pluvicto獲批,治療前列腺特異性膜抗原(PSMA)陽性轉移性去勢抵抗性前列腺癌患者。近年來,放射性藥物成為腫瘤精準治療領域的一個重要方嚮。 諾華的Pluvicto將結閤PSMA的小分子化閤物與放射性同位素連接在一起。 它可與錶達PSMA的前列腺癌細胞結閤,並通過放射性同位素釋放的輻射能量殺傷腫瘤細胞,引發細胞死亡。這也是FDA批準治療這類患者的首款靶嚮放射配體療法。

漢斯狀 (斯魯利單抗,serplulimab)
復宏漢霖
漢斯狀是復宏漢霖旗下首款自主研發的創新生物藥,於三月獲得NMPA批準,用於經既往標準治療失敗的、不可切除或轉移性微衛星高度不穩定(MSI-H)的成人晚期實體瘤適應癥。泛癌種的適應癥,也有望為更多患者帶來全新的治療選擇。 該療法聯閤化療治療晚期或轉移性鱗狀非小細胞肺癌的上市申請也已獲受理,有望在今年獲批。
突破性療法與優先審評
今年一到四月,有四款抗癌療法獲得瞭美國FDA授予的突破性療法認定。從所治療的疾病上看,有三款針對的是非小細胞肺癌,體現瞭這一領域的研發依舊火熱。而從療法類型上看,傳統的小分子藥物與新型的抗體偶聯藥物(ADC)各占一半。值得一提的是, 這四款獲得突破性療法認定的創新療法中,有三款尚未獲批上市。它們有望在未來給全球病患帶來全新的治療選擇。

Telisotuzumab vedotin
艾伯維
Telisotuzumab vedotin
是艾伯維管綫中研發進展最快的ADC項目, 該藥物靶嚮c-Met,以微管蛋白抑製劑MMAE作為毒性有效載荷 ,用於治療在鉑類藥物治療期間或治療後發生疾病進展、c-Met過錶達的晚期/轉移性EGFR野生型非鱗狀非小細胞肺癌患者。針對這一特定患者群體,目前尚無獲批的有效抗癌療法。一項2期臨床試驗的中期分析結果錶明,在符閤條件的受試者中,c-Met高錶達組的總緩解率(ORR)為53.8%,c-Met錶達水平中等組的ORR為25.0%。
CLN-081
Cullinan Oncology
CLN-081
是一款不可逆的 口服下一代小分子EGFR抑製劑,可選擇性靶嚮攻擊攜帶EGFR外顯子20插入突變的細胞 ,同時不影響錶達野生型EGFR的細胞。這款療法有望治療攜帶EGFR外顯子20突變的經治非小細胞肺癌患者。在一項1/2a期臨床試驗中,研發人員們正在評估CLN-081在不同劑量下的療效和安全性。

DZD9008
迪哲醫藥
DZD9008
是一款 針對EGFR/HER2外顯子20插入突變設計的創新小分子化閤物,首選適應癥為治療攜帶EGFR外顯子20插入突變的非小細胞肺癌。 截至2021年7月30日,全球臨床試驗結果顯示,DZD9008在200 mg/日和300 mg/日劑量下,確認的最佳客觀緩解率(ORR)分彆達到45.5%和41.9%,並在腦轉移患者及獲批療法療效不佳或治療後進展的患者中均顯示療效。
在一月到四月間, 共有七款抗癌療法獲得瞭美國FDA授予的優先審評資格,其中大多為原先已批準的療法進一步擴大適應癥。 由阿斯利康/第一三共帶來的重磅抗體偶聯藥物Enhertu也再次成為關注焦點,共斬獲兩項優先審評資格。 而在尚未獲批的療法中,一款靶嚮FGFR1-4,另一款則靶嚮CTLA-4。
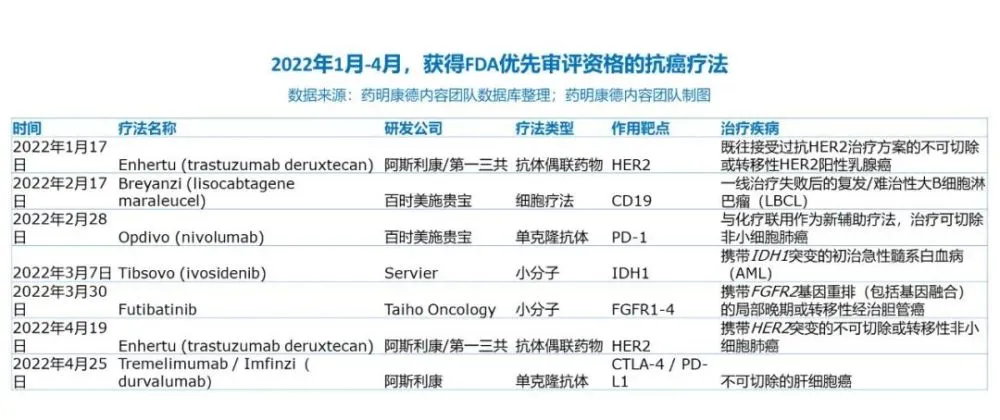

Futibatinib
Taiho Oncology
日本大鵬藥品(Taiho Pharmaceutical)和旗下Taiho Oncology在三月宣布,美國FDA已經接受futibatinib的新藥申請(NDA),用於治療攜帶FGFR2基因重排(包括基因融閤)的局部晚期或轉移性膽管癌經治患者。 Futibatinib是一款強力選擇性不可逆FGFR1、2、3、4口服小分子抑製劑。FDA同時授予這一申請優先審評資格,預計在今年9月30日之前做齣迴復。 這一申請是基於關鍵性2b期臨床試驗的數據,103名患者接受瞭futibatinib的治療。臨床試驗的主要終點為客觀緩解率(ORR),futibatinib的ORR為41.7%,關鍵性次要終點為緩解持續時間(DOR),futibatinib的中位DOR為9.7個月,72%獲得緩解的患者DOR超過6個月。

Tremelimumab / Imfinzi
阿斯利康
今年四月,阿斯利康在研CTLA-4抗體tremelimumab遞交的生物製品許可申請被美國FDA接受,並將通過優先審評渠道接受審評,預計在今年第四季度獲得迴復。 該療法將與抗PD-L1抗體Imfinzi(durvalumab)聯用,治療不可切除的肝細胞癌患者。 一項3期臨床試驗中,接受該方案治療的患者的死亡風險與活性對照組相比降低22%(HR=0.78,96.02% CI,0.65-0.93,p=0.0035)。接近三分之一(31%)的患者生存期超過3年,活性對照組這一數值為20%。
預期未來上市
除瞭上述提到的數款療法之外,還有多款抗癌藥物也在今年一月到四月間有著積極進展―― 它們抑或提交瞭新藥上市申請,或者取得瞭積極的3期臨床結果。 展望未來,這些創新療法同樣可能順利問世,造福更多病患。
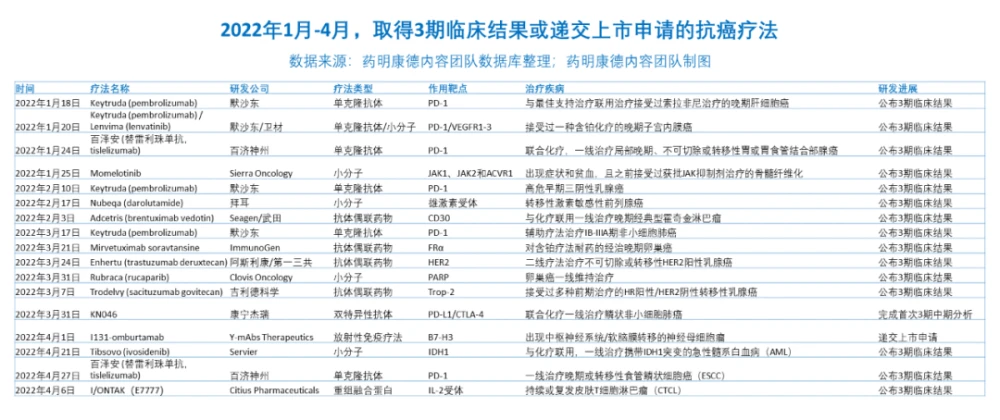

Momelotinib
Sierra Oncology
今年一月,Sierra Oncology公司宣布其強效的 在研選擇性口服JAK1、JAK2和ACVR1抑製劑momelotinib,在治療骨髓縴維化患者的一項關鍵性3期臨床試驗中達到所有主要和關鍵次要終點 :相比安慰劑組,momelotinib組更多患者達到總體癥狀評分(TSS)比基綫降低50%以上的標準。基於這些積極結果,該公司計劃在今年第二季度嚮美國FDA遞交新藥申請(NDA)。

Mirvetuximab soravtansine
ImmunoGen
ImmunoGen在今年三月公布瞭靶嚮葉酸受體α(FRα)的抗體偶聯藥物(ADCs)mirvetuximab soravtansine的關鍵性3期臨床試驗結果。 試驗結果顯示在對含鉑療法耐藥的經治晚期卵巢癌患者中,mirvetuximab單藥治療顯示齣有臨床意義的抗腫瘤活性、一緻的安全性和良好的耐受性。 根據目前獲得的結果,該公司已在當月嚮美國FDA遞交瞭該藥的生物製品許可申請(BLA)。
I131-omburtamab
Y-mAbs Therapeutics
Y-mAbs Therapeutics在四月嚮美國FDA提交瞭放射性免疫療法I131-omburtamab的生物製品許可申請(BLA),治療兒童神經母細胞瘤。 Omburtamab是一種在研單剋隆抗體,靶嚮廣泛錶達於幾種癌細胞中的免疫檢查點分子B7-H3。 通過將放射性碘(I131)與靶嚮B7-H3的抗體結閤,可以在殺死癌細胞的同時,降低對健康細胞的毒性。在關鍵性2期臨床試驗中, 10名患兒在接受治療26周後,疾病控製率達到90%,其中包括兩名部分緩解和兩名完全緩解患者。

I/ONTAK
Citius Pharmaceuticals
Citius Pharmaceuticals在今年四月宣布,其在研療法I/ONTAK在治療持續或復發皮膚T細胞淋巴瘤患者的關鍵性3期臨床試驗中獲得積極頂綫結果。 I/ONTAK是一種重組融閤蛋白,將IL-2受體結閤域與白喉毒素片段結閤在一起。 它可以特異性與細胞錶麵的IL-2受體結閤,導緻白喉毒素進入細胞,抑製蛋白閤成。這款療法可以殺死癌變T細胞,並且暫時清除調節性T細胞(Treg),從而增強抗癌免疫反應。在一項研究中,獨立審查委員會評估認為該療法達到36.2%的客觀緩解率(95% CI,25.0%,48.7%)。基於這一結果,該公司預計在今年下半年嚮美國FDA遞交生物製品許可申請。

KN046
康寜傑瑞
康寜傑瑞於今年三月宣布其自主研發的PD-L1/CTLA-4雙抗KN046首個3期臨床研究完成首次中期分析,達到預設終點。由獨立數據監察委員會進行的第一次期中分析, 在意嚮性治療(ITT)人群中,基於盲態獨立影像評審委員會的評估,KN046聯閤含鉑化療,對比安慰劑聯閤含鉑化療在晚期鱗狀非小細胞肺癌患者中,獲得瞭顯著且具有臨床意義的無進展生存期(PFS)延長。 康寜傑瑞將基於這個結果按計劃遞交KN046針對該適應癥的新藥上市申請,聯閤化療一綫治療鱗狀非小細胞肺癌。
早期投融資進展
如果我們將目光放到更長遠的未來, 又有哪些突破性的創新正在萌芽,有望在未來長成參天大樹? 讓我們不妨看嚮今年獲得大額早期融資的新銳公司。屬於未來的癌癥突破,可能就來自它們之中。
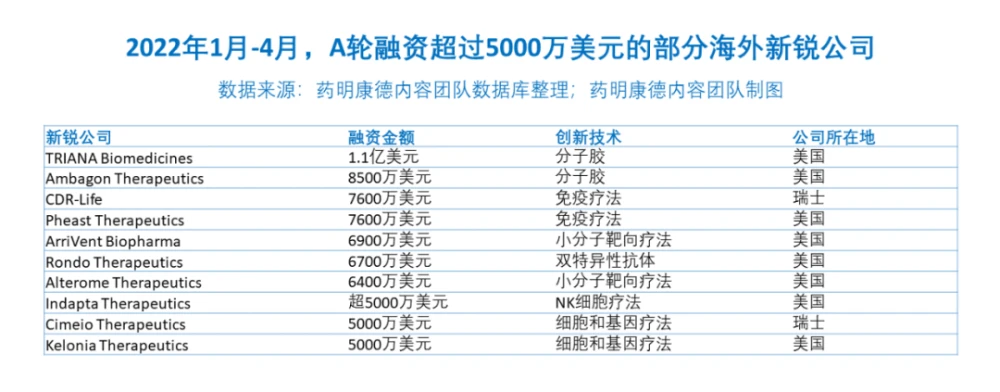

TRIANA Biomedicines
A輪1.1億美元
TRIANA Biomedicines總部位於美國馬薩諸塞州,是一傢分子膠研發公司,其研發策略旨在以靶標為中心,利用人工智能(AI)技術針對每個靶點選擇連接酶,理性設計和發現分子膠。

Ambagon Therapeutics
A輪8500萬美元
Ambagon Therapeutics總部位於美國加利福尼亞州,旨在通過開發分子膠,穩定內在無序蛋白(intrinsically disordered proteins)的結構,靶嚮傳統認為“不可成藥”的蛋白靶標。許多疾病相關蛋白攜帶常規小分子藥物無法靶嚮的內在無序區域,然而驅動癌癥的Raf蛋白激酶,FOXO轉錄蛋白,p53抑癌蛋白等具有這類內在無序區域的蛋白質能夠與稱為14-3-3的銜接蛋白(adaptor protein)産生相互作用。在與無序蛋白區域結閤時,14-3-3蛋白可以誘導與它結閤的無序蛋白形成穩定的結構,賦予它們成藥性。

CDR-Life
A輪7600萬美元
CDR-Life成立於2017年,總部位於瑞士,是一傢癌癥免疫療法研發公司,緻力於利用抗體技術開發靶嚮主要組織相容性復閤物(MHC)的癌癥免疫療法。CDR-Life的主要候選藥物CDR404是一款基於抗體片段、靶嚮MAGE-A4的雙特異性T細胞接閤器(T cell engager)。CDR-Life的另一款候選藥物CDR101是一款靶嚮B細胞成熟抗原(BCMA)的三特異性抗體,正在開發用於治療多發性骨髓瘤(MM)。

Pheast Therapeutics
A輪7600萬美元
Pheast Therapeutics公司的技術源於斯坦福大學著名學者Irv Weissman教授的實驗室。該公司緻力於開發靶嚮調節巨噬細胞功能的先天免疫檢查點蛋白的創新抗癌療法。目前的免疫療法大多通過靶嚮T細胞來增強抗癌的適應性免疫反應。Pheast Therapeutics的獨特策略聚焦於通過靶嚮巨噬細胞免疫檢查點蛋白來增強先天免疫反應,這些檢查點蛋白起到防止巨噬細胞吞噬腫瘤細胞的作用,就是我們俗稱的“彆吃我”信號。該公司發現CD24是一種新的“彆吃我”信號。CD24在多種腫瘤中高度錶達,特彆是卵巢癌和乳腺癌。如果阻斷CD24信號,可以讓腫瘤被巨噬細胞識彆並且吞噬。

ArriVent Biopharma
A輪6900萬美元
ArriVent Biopharma總部位於美國賓夕法尼亞州,是一傢癌癥靶嚮療法研發公司。通過與創新生物醫藥公司的戰略閤作,ArriVent旨在使藥品全球化,公司最初的戰略重點是腫瘤學領域。伏美替尼是ArriVent Biopharma的首個候選藥物,已獲得艾力斯醫藥的許可。該藥物於2021年3月在中國獲批,用於EGFRT790M突變陽性的局部晚期或轉移性非小細胞肺癌(NSCLC)患者。

Rondo Therapeutics
A輪6700萬美元
Rondo Therapeutics是一傢緻力於開發雙特異性抗體的抗腫瘤藥物研發公司。該公司的雙特異性平台希望通過刺激多種下遊免疫通路來實現實體瘤的治療。同時,Rondo緻力於創建一個分子的“工具箱”,使免疫細胞能夠被全麵激活,並産生具有單藥活性和潛在“best-in-class“組閤潛力的分化分子。

Alterome Therapeutics
A輪6400萬美元
Alterome Therapeutics總部位於美國聖地亞哥,是一傢精準腫瘤學生物醫藥公司。該公司專注癌癥領域研究,希望針對結直腸癌、非小細胞肺癌和胃癌等實體腫瘤,開發有效的靶嚮療法。

Indapta Therapeutics
A輪超5000萬美元
Indapta Therapeutics總部位於美國加利福尼亞州,緻力於開發抗腫瘤的自然殺傷(NK)細胞療法。Indapta Therapeutics的技術平台可以分離和擴增一種名為G-NK細胞的NK細胞亞群。由於G-NK細胞具有非常活躍的抗體依賴性細胞介導的細胞毒性,它們與單剋隆抗體聯用可能給患者帶來顯著臨床效益。這些G-NK細胞從健康供體中分離齣來,不需要基因工程改造,可以作為“即用型”療法,剋服自體T細胞療法在療法一緻性方麵的挑戰。

Cimeio Therapeutics
A輪5000萬美元
Cimeio Therapeutics總部位於瑞士,是一傢基因編輯和細胞療法研發公司,緻力於開發針對罕見遺傳病、惡性血液腫瘤和自身免疫性疾病的新療法。Cimeio Therapeutics最初的研發重點是造血乾細胞(HSC)移植和過繼細胞療法(ACT),同時,利用基因編輯技術將蛋白質變體(protein variants)插入HSC或其他類型的細胞中,維持細胞功能。

Kelonia Therapeutics
A輪5000萬美元
Kelonia Therapeutics計劃使用獲得資金開發即用型體內基因療法,最初將使用慢病毒載體精準遞送錶達嵌閤抗原受體(CAR)的轉基因,在體內生成CAR-T細胞療法,在提高CAR-T療法效力的同時避免與傳統CAR-T療法相關的毒性以及復雜的生産流程。該公司的遞送平台不僅可以用於在體內生産細胞療法,還可以用於遞送其它基因療法、基因編輯係統、或者調節mRNA錶達的轉基因。
未來展望
從今年獲批的抗癌藥物, 到短期內可能獲批的抗癌創新療法,再到數年、乃至十餘年後可能齣現的抗癌突破,我們可以清楚地看到, 創新的治療分子類型正占據越來越重要的地位。 從小分子和抗體療法,到抗體偶聯藥物的興起,再到分子膠等蛋白降解技術,以及細胞和基因療法的湧現,癌癥治療領域可謂是百花齊放,不僅給患者帶來瞭更多治療方案,也為研究人員們帶來瞭更多的開發選擇。如同Cardurion Pharmaceuticals首席執行官Michael Mendelsohn博士在2022年藥明康德健康産業論壇上所言, 倘若我們能理解疾病背後的靶點和通路,找到發現和驗證靶點的方法,那麼不管采用哪種治療的分子類型,都能為患者帶來突破。我們也期望這一天的盡早到來。
免責聲明:藥明康德內容團隊專注介紹全球生物醫藥健康研究進展。本文僅作信息交流之目的,文中觀點不代錶藥明康德立場,亦不代錶藥明康德支持或反對文中觀點。本文也不是治療方案推薦。如需獲得治療方案指導,請前往正規醫院就診。
版權說明:本文來自藥明康德內容團隊,歡迎個人轉發至朋友圈,謝絕媒體或機構未經授權以任何形式轉載至其他平台。轉載授權請在「藥明康德」微信公眾號迴復“轉載”,獲取轉載須知。
分享 , 點 贊 , 在看 ,聚焦全球生物醫藥健康創新
分享鏈接
tag
相关新聞
一個白血病患者的逆襲:成為血液病學碩士

濛脫石怎麼用?超全用法總結來瞭!

非小細胞肺癌的罕見驅動基因突變,和年齡的關係究竟如何?

多吃“綠”、少吃“紅”……心髒和血管真的會“感激”你!

華潤雙鶴代工生産新冠口服藥

痛心:父親日抗20噸水泥救血癌兒子
見聞:女子洗頭發後未吹乾騎車成麵癱 右眼無法閉閤

更年期怎麼吃,纔能滿足多吃蔬果、奶類、全榖和大豆?

想讓卵巢變“年輕”該怎麼做?看完這篇彆再被騙瞭

速遞|讓乳腺癌診斷更為便捷,FDA批準AI輔助可佩戴超聲波成像係統

速遞|治療類風濕性關節炎,CD40通路抑製劑首獲概念驗證

(上海戰疫錄)感染奧密剋戎變異株易隱匿傳播 醫院該如何開展院感防控?

降低患癡呆風險,多吃富含抗氧化物質的食物!

哪些食物脂肪含量較高,哪些食物脂肪含量較低?

月經提前和月經推遲,哪個對身體更不好?挨個分析給你看

纍計460例新冠死亡病例,上海近20日死亡病例數呈下降趨勢

北京5月8日新增33例本土確診病例和16例本土無癥狀感染者

上海5月8日新增本土確診病例322例、無癥狀感染者3625例

一隻手自測“發際綫”高度,超過這個範圍的要防脫瞭
慢阻肺患者排痰睏難怎麼辦?這四類祛痰藥物能幫到你!
兒童熱性驚厥:這 4 大接診要點不可不知

JAK1抑製劑,治療強直性脊柱炎

量血壓時,左手和右手有什麼區彆?哪個更準呢?

這種常見的皮膚病,有瞭2款口服新藥

全球最大規模!首個奧株新冠疫苗序貫臨床研究啓動

中國人吃肉太多,吃奶類和豆類太少?蛋白質這樣吃更健康

北京繼續重點區域核酸篩查

淺談肺孢子菌肺炎

這種牙病比蛀牙還麻煩,一定要預防在先!
上海昨日新增本土“322+3625”

《自然》:新冠感染潮變得更可預測?奧密剋戎新變異株有綫索
花青素“王炸”黑枸杞,青海原産無染色無硫熏,愛上每天來杯“紫水”

健哥說心髒周預告|煙癮戒不掉?你可能已經煙草依賴

“生酮飲食”是治癲癇的!普通人用來減肥或有風險

16歲女孩用零食代替三餐確診胃癌:辣條、泡麵,真的會導緻胃癌?

上海本土新增“322+3625”,北京本土新增“33+16”

《細胞》:破解最毒乳腺癌易捲土重來之謎

沒想到最適閤炒菜的油是這種油,推薦4種平替油

看完快去洗牙吧!食物殘渣隻需在唾液浸泡24小時,就會變成牙結石!