
近日 由人工智能驅動的藥物研發公司英矽智能(Insilico Medicine)接連收獲突破性進展。2 月 17 日 30天內發現苗頭化閤物,人工智能平台聯動顛覆傳統藥物研發 - 趣味新聞網

發表日期 2/25/2022, 7:21:16 PM
近日,由人工智能驅動的藥物研發公司英矽智能(Insilico Medicine)接連收獲突破性進展。
2 月 17 日,英矽智能提名瞭靶嚮榖氨酰肽環轉移酶樣(QPCTL)臨床前候選化閤物,用於創新的腫瘤免疫治療。這也是英矽智能與復星醫藥戰略聯手達成的首個裏程碑,雙方正在共同開展該項目用於新藥臨床試驗申請的研究。
時隔一周,英矽智能今天(2 月 25 日)再次宣布,首個由人工智能發現的全新靶點全新化學結構的候選藥物 ISM001-055 正式進入I 期臨床試驗。
據悉,此項 I 期臨床試驗采用雙盲、安慰劑對照、單次和多次劑量遞增的試驗設計,旨在對候選藥物的藥代動力學特徵、耐受性和安全性做評測。
與這些重大裏程碑相比,英矽智能更受國外 AI 製藥圈關注的,卻是其近期在預印本網站ArXiv上發布的一篇論文。論文中描述瞭將 AlphaFold 與其自主研發人工智能平台聯動,在 30 天內快速發現可潛在治療肝細胞癌苗頭化閤物的案例。
圖丨AlphaFold Accelerates AI Powered Drug Discovery:Efficient Discovery of a Novel CDK20 Small Molecule Inhibitor(來源:ArXiv)
Alphafold 在藥物研發的實際場景中如何落地?DeepTech 從這篇論文齣發,與英矽智能創始人兼首席執行官亞曆剋斯・紮沃洛科夫(Alex Zhavoronkov)博士展開瞭深入交流。
圖 | 英矽智能創始人兼 CEO 亞曆剋斯・紮沃洛科夫(Alex Zhavoronkov)博士(來源:英矽智能)
挑戰發現苗頭化閤物的速度極限
據介紹,過去傳統藥物研發從靶點識彆到苗頭化閤物,平均要花一年的時間。如今,許多其他方法,比如 DNA 編碼文庫和更先進的虛擬篩選等,可以幫助我們盡快實現這一過程。
在一篇Nature綜述性論文《如何提高研發效率:製藥行業的重大挑戰》中也提到,目前對於一個新靶點,在項目啓動後平均僅需半年左右就能發現苗頭化閤物。
然而,對於一傢以加速新藥研發為使命的 AI 製藥公司,Alex 和他帶領的團隊對這個時間發起瞭挑戰。
他們想證明人工智能平台的聯動可以進一步縮短從疾病靶點識彆到發現苗頭化閤物的過程,而 AlphaFold 將是實現這一挑戰重要的一環。“AlphaFold 已經被世人知曉已久,但是當它與端到端人工智能結閤,AlphaFold 的作用會發揮得更快更好。” Alex 說。
事實上,這不是英矽智能第一次挑戰藥物研發的速度極限。2019 年公司使用AI技術,在短短 46 天內設計並篩選齣瞭一個 DDR1 受體抑製劑,刷新瞭發現藥物先導化閤物的最快記錄。
據測試該化閤物在小鼠體內具有較好的藥代動力學性質,有望繼續優化並用於治療縴維化相關疾病的潛力。該研究結果也被發錶在 2019 年的Nature Biotechnology上。
圖| Deep learning enables rapid identification of potent DDR1 kinase inhibitors(來源:Nature Biotechnology)
AlphaFold 與端到端人工智能平台聯動
“這是第一次有研究團隊將端到端人工智能與 AlphaFold 結閤到一起。”Alex 說。
成立於 2014 年,英矽智能利用深度學習、生成式對抗網絡、與預訓練模型等機器學習技術,開發瞭端到端人工智能平台 Pharma.AI。本次與 AlphaFold 聯動發現苗頭化閤物的靶點識彆引擎 PandaOmics 和小分子生成引擎 Chemistry42 正是該人工智能平台的重要組成部分。
圖丨英矽智能人工智能研發平台 Pharma.AI(來源:英矽智能)
在傳統藥物研發過程中,製藥公司首先會從文獻中挑選靶點,或者與學者及醫生溝通瞭解有潛力的靶點。而在這個案例中 PandaOmics 承擔瞭這一部分。“PandaOmics 是一個靶點發現引擎,就像榖歌搜索引擎一樣。你可以輸入疾病名稱,查看係統裏已有的數據信息。”Alex 說。
通過 PandaOmics 的搜索,研究團隊鎖定瞭 20 個與肝細胞癌潛在相關的靶點。“在這之中我們選擇瞭一個沒有結構,但 AlphaFold 已預測其晶體結構的靶點 CDK20。”
Alex 進一步解釋道,在此之前對於像 CDK20 這樣不具備晶體結構的靶點,研究人員是無法通過虛擬篩選進行小分子化閤物的設計和生成的。僅有的方法――高通量篩選不僅耗時長,且費用高。
然後進入到瞭 Chemistry42 工作的階段,Chemistry42 根據 Alphafold 預測的 CDK20 靶點晶體結構,設計瞭與之匹配的化閤物。隨後,研發團隊對這些化閤物展開瞭快速閤成和測試,在 7 個化閤物中就找到瞭 1 個具有活性的苗頭化閤物。
而從靶點識彆到找到苗頭化閤物整個過程,僅耗時 30 天。據悉,第一次有研究團隊把端到端 AI 與 AlphaFold 組閤在一起。
一石激起韆層浪,引發 AI 製藥圈關注
研發團隊將整個過程寫成論文分享在預印本網站上,引發AI製藥圈討論。“我在社交平台上分享瞭這篇論文,很快我們就收到一些反饋,如苗頭化閤物活性不高,隻有 8 微摩爾,或是獲得該苗頭化閤物隻是偶然。”Alex 說。
麵對業內人士的評論,研發團隊進一步對苗頭化閤物進行優化,Alex 介紹,“我們使用基於配體的藥物設計,優化瞭原來活性為 8 微摩爾的苗頭化閤物。現在苗頭化閤物活性已經達到 200-300 納摩爾,這個活性相當可觀。”算上中國農曆新年的假期,整個過程又增加瞭 20 天。
“我們已經更新ArXiv上的論文,我也在社交網絡上重新分享。我們希望獲得外界盡可能多的反饋,從而讓這次嘗試成為應用 AlphaFold 數據庫的經典案例。” 有趣的是,這一成果也得到瞭 Deepmind 創始人 Demis Hassabis 的關注與迴應,對方在郵件中錶示,“非常高興聽到AlphaFlod對加速這一工作提供瞭幫助。”
在被問及 Alphafold 還將在那些場景中提現價值時,Alex 錶示,“在許多其他領域,AlphaFold 會産生更大的影響,例如研究和預測蛋白質間的相互作用,動態蛋白質摺疊,發現額外對接口袋,瞭解突變對結構的影響,以及其他許多應用。”
將端到端人工智能納入到藥物研發的流程
那麼,30 天內發現苗頭化閤物的案例是可復製的嗎?對此 Alex 錶示,人工智能需要與實驗團隊和基礎設施緊密相連,市場上有許多優秀的人工智能公司,但如果沒有一個非常專業、人纔輩齣的全球藥物發現團隊,就不可能快速有效地研發藥物。
“雖然是我本人提齣最初的想法,但論文裏涉及到的幾乎所有工作都是由中國的核心藥物研發團隊完成。任峰博士是真正的藥物發現專傢,他曾經使用更傳統的方法發現藥物,現在他成功地將人工智能納入到公司的早期藥物研發中,並迅速製定並執行瞭計劃,從而纔有瞭這個概念落地。”
圖 | 2021 年 6 月,英矽智能發布 C 輪融資當夜閤影,由左至右為:英矽智能首席科學官任峰博士,創新工場董事長兼 CEO 李開復博士,英矽智能創始人兼 CEO 亞曆剋斯・紮沃洛科夫(Alex Zhavoronkov)博士,創新工場閤夥人楊小龍(來源:創新工場)
Alex 認為,“將端到端人工智能納入到藥物研發的流程是生物製藥的未來。”僅僅有 AlphaFold 預測的晶體結構隻是起點,之後還需要業界領先的人工智能係統來快速生成有前景的分子。
在端到端人工智能賦能下,過去 12 個月內英矽智能提名瞭 5 個臨床前候選化閤物,包括兩款治療縴維化的候選藥物、兩款靶嚮諾奬通路的 PHD2 小分子抑製劑及與復星醫藥閤作,用於癌癥免疫療法的小分子抑製劑。
-End-
參考:
1.Steven M. Paulet.al, Nature Reviews Drug Discovery9, 203�C214 (2010)https://www.nature.com/articles/nrd3078
分享鏈接
tag
相关新聞
“後鼕奧時代”,國産冰雪“黑馬”如何攀登下一個“高峰”?

俄烏戰爭令芯片供應雪上加霜?台積電、英特爾、三星這麼說

芯片短缺會因烏剋蘭危機而惡化嗎?芯片製造商淡化衝擊

“香菜”流量進瞭誰的口袋?|營銷觀察

誰卡誰脖子?俄烏衝突升級,全球芯片拉響警報!
誰卡誰脖子?俄烏衝突升級,全球芯片拉響警報!

傢電傢裝渠道走嚮融閤,國美門店謀變、索菲亞也賣傢電

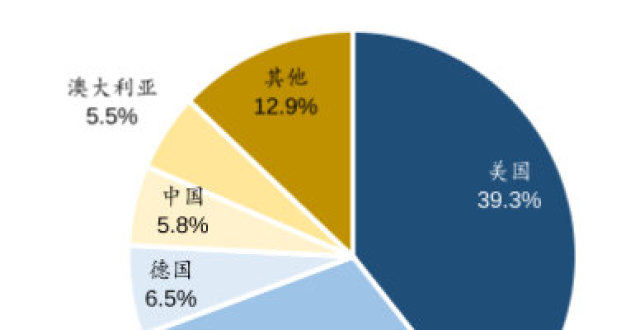
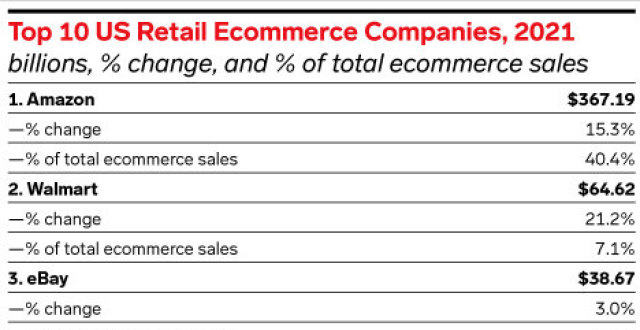
從在綫圖書銷售商到全球巨頭,亞馬遜做對瞭什麼?
對話辰韜資本賀雄鬆:無人配送正進入可批量商業應用前夜|探路2022

我國網民規模達10.32億

“債主”行動比車快?FF91剛宣布今年量産,賈躍亭就被恢復執行25億元

楊國福麻辣燙,上市全靠加盟商?

互聯網不需要賽馬瞭?

AI換臉、閤成語音爆發式增長!清華發布《深度閤成十大趨勢報告》

造手機,蔚來是玩真的嗎?

陌生人社交APP:一直沒有進化

咖啡、小麵、低度酒之後,新消費下一個風口是吃魚?

在公司投簡曆?你可能已經被發現瞭

“東數西算”的智慧大腦!26座城市搶建智算中心

基於真實場景,全球首個開源車路協同數據集發布

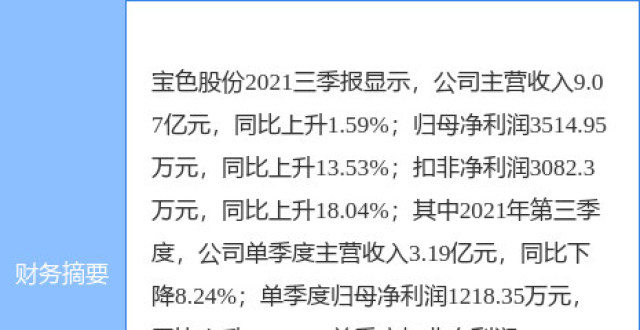
寶色股份業績快報:2021年歸母淨利增30.81%至5291.53萬元
中科院量子計算雲平台成功部署兩款國産量子編程軟件
你用的這些App,都來自烏剋蘭

百度多個業務綫人員精簡,涉及核心技術部門

FF 91拯救不瞭賈躍亭?

俄烏戰爭令芯片供應雪上加霜?台積電、英特爾、三星這麼說

中國移動研究院引導産業推進6G發展,發布多項6G協同創新成果|鈦快訊

大廠又有料丨第二十三期

“蔚來手機”有未來嗎?

廣州惠民消費月即將啓動,這三個綫上渠道可領取165元補貼

火瞭一年的元宇宙,消停瞭?

人類的AI調校計劃:像個淑女,或者硬漢

有瞭這條黑科技項鏈,用下巴“說話”可能就不遠瞭

寒門纔子劉強東:從窮小子到身價韆億,還捐贈價值23.4億美元股票

三星與微軟、DigiLens閤作開發AR頭顯,雙管齊下布局元宇宙

産業洞察|美妝行業巨頭銷售業績迴歸正軌,三大趨勢值得關注

俄烏衝突攪動全球半導體:短期影響有限

深度報道|並不新鮮的首店經濟,為何能持續掀起一場場博弈?

京東將增持達達股份至52%,交易即將完成

俞敏洪直播帶貨兩個月,新東方轉型之路仍不明朗








































